Glycogen グリコーゲン
- 概要: グリコーゲンとは
- グリコーゲンの分解
- Glycogen phosphorylase
- Phosphoglucomutase
- Transferase/α-1,6-glucosidase
- G6P の運命 - Glucose 6-phosphatase
- 分解の制御: See glycogen phosphorylase
- グリコーゲンの合成
概要: グリコーゲンとは
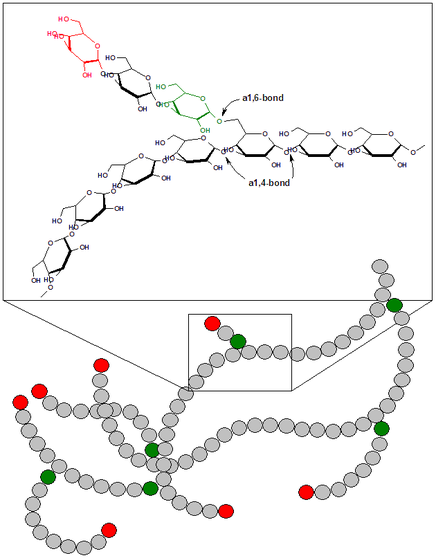
グリコーゲン glycogen とは,グルコース glucose が α-1,4- および α-1,6-グリコシド結合 glycosidic bond によって重合した高分子である(図, 文献 1)。動物の主要な貯蔵糖質である。
> α-1,6-glycosidic bond が入るところで分岐する(2)。
: 分岐はおよそ 10 のグルコースにつき 1 回入る。
: α-グリコシド結合は,セルロースを構成する β-グリコシド結合よりも折れ曲がっている。
: ゆえにセルロースはグリコーゲンよりも繊維状である。
: 枝分かれのメリット → 溶解度と分解の効率が上がる。
> 哺乳類では,主なグリコーゲン貯蔵組織は肝臓および骨格筋である(2)。
: 細胞質に直径 10 - 40 nm の顆粒の形で存在する。
グリコーゲンの分解
グリコーゲンの分解は,以下の 3 つの段階から成る(2)。4 つの酵素 enzyme が必要である。
- グリコーゲンからグルコース-1-リン酸 glucose-1-phosphate (G1P) が遊離する。
- グリコーゲンは,さらなる分解のために構造変化を起こす。
- G1P がグルコース-6-リン酸 glucose-6-phosphate (G6P) に変換される。
グリコーゲンホスホリラーゼ
グリコーゲンホスホリラーゼ glycogen phosphorylase は,グリコーゲンに無機リン Pi を付加して G1P を遊離させる(1,図は文献 3)。この酵素は,リン酸化と AMP による制御を受けている。詳細はリンク先を参照のこと。ホルモンなどによるグリコーゲン分解の制御についても,glycogen phosphorylase のページでまとめている。
Glycogen + Pi → Glucose-1-phosphate + Glycogen (1 残基短い)

G1P は非還元末端(Carbon 4 の OH 基が残っている側) から遊離する。
> 切り取る際に,なぜわざわざリン酸化するのか? - いくつかのメリットがある(2)。
: 解糖系に入る際に,ATP を消費しなくてすむ。
: グリコシド結合を加水分解すればグルコースが得られるが,解糖するには ATP でリン酸化しないといけない。
: エネルギー準位の近いグリコシド結合とリン酸エステル結合を使えば,ATP のかわりに Pi でリン酸化可能。
: 細胞内に豊富にある Pi を有効利用しているとも言える。
: さらに,筋肉の場合,グルコースが遊離するとトランスポーターを通って細胞外に出てしまう。
: G1P ならトランスポーターがないので,自分で分解に回せる。
> この反応を達成するためには,活性部位に水を排除しつつ Pi を引き込まねばならない(2)。
: これを可能にするメカニズムが構造解析で詳細に調べられている。
ホスホグルコムターゼ
G1P を G6P に変換する酵素は ホスホグルコムターゼ phosphoglucomutase である(2)。ムターゼ mutase は英語では [mjuːteiz] と発音し,リン酸基などの分子内転移を触媒する酵素のことをいう。
解糖系の phosphoglycerate mutase (PGM) と混同しないように注意すること。
トランスフェラーゼと α-1,6-グルコシダーゼ
Glycogen phosphorylase は α-1,6-グリコシド結合を切ることができない。また,α-1,6-グリコシド結合による分岐があると,その 4 残基手前で α-1,4-グリコシド結合の切断も止まってしまう(2)。
その場合,transferase が 3 つの残基を下の図のように移し替えることで,α-1,4-グリコシド結合が切断されるようになる。1 個だけ残った α-1,6-グリコシド結合による分岐は,α-1,6-glucosidase で切断される(1)。これは加水分解であり,G1P でなくグルコースが生じる。
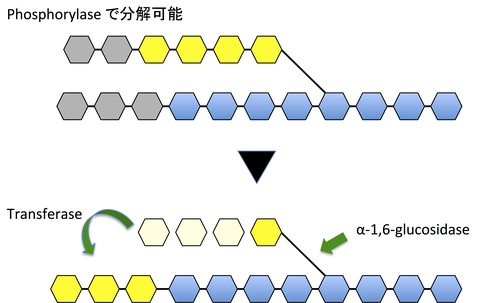
> Transferase と α-1,6-glucosidase は,1 本のポリペプチド上に存在する bifunctional enzyme である(1)。
: 解糖系フラックスを調節する PFK2 も kinase と phosphorylase の bifunctional enzyme である。
G6P の運命 - glucose 6-phosphatase
G6P は解糖系の中間代謝産物であるとともに,ペントースリン酸経路の出発点でもある。G6P は,以下の 3 通りのパターンで代謝され得る(2)。
- 解糖系でピルビン酸まで代謝される。
- 解糖系を逆行し,グルコースになる。この反応は主に肝臓で起こり,glucose 6-phosphatase によって触媒される。この酵素は,ほぼ肝臓のみで発現している。
- ペントースリン酸経路で代謝される。この経路は NADPH とリボース ribose の類縁体を合成するための経路である。
グリコーゲンの合成
グルコースをグリコーゲン鎖の末端に付加するためには,uridine-diphosphate (UDP) と結合させ,活性化された状態にしなければならない(2)。UDP-glucose はグルコース-1-リン酸 glucose-1-phosphate (G1P) と UTP から作られる。
Glucose-1-phosphate + UTP → UDP-glucose + PPi
リン酸基が 2 つ外れることに注意する。グリコーゲン合成は
Glycogen + UDP-glucose → Glycogen (1 残基長い) + UDP
である。この反応は グリコーゲン合成酵素 glycogen synthase に触媒される(2)。UDP は,ATP のリン酸基を使って UTP にリサイクルされる。
> Glycogen synthase は,4 残基以上の既存の glycogen を伸長する酵素である(2)。
: α-1,4-グリコシド結合のみを作る。α-1,6-グリコシド結合による枝分かれは branching enzyme が作る。
> Glycogen synthase は PKA および glycogen synthase kinase (GSK) にリン酸化され,不活性化する(2)。
: グリコーゲン分解の glycogen phosphorylase は,PKA によって活性化する。
: つまり,PKA は 合成の停止 と 分解の開始 を同時に行う。
> GSK はインスリンによって活性化される(2)。
References
- パブリック・ドメイン, https://commons.wikimedia.org/w/index.php?curid=611992
- Berg et al. Biochemistry: 使っているのは 6 版ですが 7 版を紹介しています。
- By Biochemnerd1 - Own work, CC BY 3.0 us, https://commons.wikimedia.org/w/index.php?curid=15226222