リポタンパク質リパーゼ, Lipoprotein lipase, LPL
2022/12/20 Last update
このページは リポタンパク質リパーゼ @本家UBサイト に恒久的に移転しました。このページもネット上に残っていますが、最新の情報はリンク先を参照して下さい。
- 概要
- 構造
- 全体的な特徴
- 活性部位
- ヘパリン結合部位
- 基質結合部位
- システイン残基
- 酵素活性
- 発現部位
- リガンドとしての機能
概要: リポタンパク質リパーゼとは
いわゆる「脂肪」であるトリアシルグリセロール TG (右図)は,グリセロール1分子(青い部分)と脂肪酸(黒い部分)3分子がエステル結合した分子である。
脂肪組織や肝臓にエネルギー源として貯えられており,必要に応じて筋肉などに血液を介して輸送される。
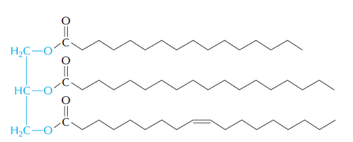
トリアシルグリセロールの一例(文献7より)。
TG の水溶性は非常に低いため,血液を介した輸送の際には,タンパク質やリン脂質の複合体であるリポタンパク質 lipoprotein として存在する。
しかし,リポタンパク質はそのままでは細胞膜を通ることができないため,細胞に取り込まれる際には以下の2つのいずれかの方法をとる必要がある。
- 脂肪酸部分が リポタンパク質リパーゼ lipoprotein lipase (LPL) による加水分解で切り離され,生じた遊離脂肪酸 NEFA が脂肪酸トランスポーターを通して取り込まれる。
- リポタンパク質が細胞膜上の受容体に結合し,受容体ごとエンドサイトーシスされる。
LPL (EC 3.1.1.34) は 1. の加水分解を触媒する酵素で,組織への脂質の取り込みを制御する機能をもっている。LPL は,血液から組織に脂質が分配される lipid partitioning に重要(LPL
活性が高い組織ほど,たくさん脂質を取り込む)ため,盛んに研究が行われている。また,2. の反応においてもリポタンパク質の認識に関わるリガンドとしての役割を果たしている(11)。 血液に接している LPL を functional LPL ということもある(14)。
脂質を血液から細胞内へ移行させるのが基本的な機能であるため,血中脂質が高い状態で働くと考えられる。インスリン insulin による制御が有名である(LPL の発現調節へ)。
構造
LPL 自体の立体構造解析は行われていないが,膵臓リパーゼ pancreatic lipase の構造をもとに議論がなされている。
全体的な構造上の特徴
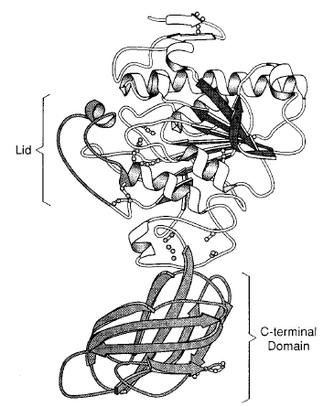
右図(3, ヒトLPL)のように,大きく N 末端ドメインと C 末端ドメインに分かれる。
N 末端ドメインは酵素の活性に,C 末端ドメインは基質特異性に寄与するところが大きいと考えられている。
他のリパーゼ Pancreatic lipase (PL), hepatic lipase (HL), endothelial lipase (EL) などとともに,GXSXG motif の中にある Ser が活性中心である(11)。
活性部位 Active site
Ser-Asp-His がよく保存された catalytic triad である(11)。
ヘパリン結合部位 Heparin-binding site
ヘパリン結合サイトをもつ(4)。
: ヘパリン結合のコンセンサス配列 [B-B-X-B] または [B-X-B-B-X-X-B] に従う。
基質結合部位 Substrate binding site
> ヒト LPL では,415 - 438 番目のアミノ酸が,基質との結合およびダイマー形成に必要である(2R)。
: この領域には,よく保存された疎水性アミノ酸の連続領域が2ヶ所あり,基質結合部位と思われる。
: 9種の変異体を HEK293 で発現させ tributylin(水溶性),triolein(脂溶性)基質の分解をテスト。
: 基質の特性や,酵素の安定性が変化した。ダイマー形成にも影響していると考えられた。
システイン残基
> ヒト LPL では,10 個の Cys が,5 組のジスルフィド結合を形成し,構造の安定性に寄与する(8)。
: ニジマスの LPL では C-terminal domain の1組が欠けている。
: 体温が低いために,酵素がフレキシブルな構造になっていると考えられる。
: ニジマス LPL は,実際に37℃で処理したときの活性低下がウシ LPL よりも著しい。
酵素活性 Enzymatic activity
LPL は,TAG に富むリポタンパク質であるキロミクロン,VLDL 中の TAG を NEFA と 2-モノアシルグリセロールに加水分解する(1I)。生成したNEFA は,例えば脂肪組織では再エステル化されて再び TAG として保存され,筋肉では β 酸化されてエネルギー源になる。
> LPL 酵素活性の詳細 へ
- TAG の sn-1 位を優先的に加水分解する。
- ジアシルグリセロール DAG も加水分解でき,やはり sn-1 位が優先される。
- 1 M オーダーの NaCl で酵素活性が阻害される。
発現部位
> ラット肝臓では,新生児のみで mRNA 発現がみられる。成体では mRNA が発現しない(5)。
: 悪液質 cachexia (6)のときは,成体の肝臓でも発現がみられる。
> 成体ラットの脳 brain で酵素活性が検出されている(9)。
: 14C-トリオレインを基質として,1 - 2 nmol/min/g
の活性が得られている。
> ラット caudap spinal cord には,筋肉や脂肪組織と同等の酵素活性が存在する(10R)。
: 小脳 cerebellum での活性がやや高く,10 nmol/min/g。他の脳部位では 3 未満が多い。
: mRNA は海馬 hippocampus で多く,視床,大脳皮質,下垂体でも Northern で検出される。
: 免疫染色したところ,多くは脳の血管で発現。しかし gray matter をはじめ様々な部位も染まる。
: LPL活性が異なるのに,食べた14C-オレイン酸の取り込み量は脳の各部位で均一である。
> 腎臓では LPL 活性が高いが,脂肪酸取り込みは少なく,血中 FFA
pool を作っているかも(14R)。
: ミンク,ハムスター,マウス,ラット,モルモットの各組織の LPL 活性が測定されている。
: マウス腎臓の LPL 活性はサーカディアンリズムに従う。脂肪組織でも論文があるらしい。
: マウス腎臓の LPL 活性は,6時間から48時間の絶食期間中低下する。mRNA 量は変化しない。
: ヘパリン投与によって,マウス腎臓の LPL 活性は約 49% に低下。心臓ではあまり変化しない。
リガンドとしての機能
> LPL は,LDL 受容体経由のリポタンパク質の取り込みにも重要である(13R)。
: 3H-cholesteryl oleoyl ester (CE) と,14C-triolein を Intralipid でエマルジョンにして注射。
: Intralipid emulsion dropletは,脂肪酸組成と大きさがキロミクロンに似ている。
: CE は LPL の基質にならないので,3H, 14C 量の比は LPL経由:LDLR経由の取り込みの比になる。
: ヘパリンを注射すると, 14C-triolein だけでなく 3H-CE の取り込みも低下する。
: 肝臓ではヘパリン注射によってむしろ増大。他の組織から遊離した LPL が肝臓で捕捉されている?
: LPL 阻害剤 THL 注射で血中 TAG 量が増大し,肝臓よりも心臓で TAG と CE の取り込みが低下。
References
- Shan et al. 2009a. The angiopoietin-like proteins ANGPTL3 and ANGPTL4 inhibit lipoprotein lipase activity through distinct mechanisms. J Biol Chem 284, 1419-1424.
- Keiper et al. 2001a. Novel site in lipoprotein lipase (LPL415–438) essential for substrate interaction and dimer stability. J Lipid Res 42, 1180-1186.
- Dugi et al. 1995a. Human hepatic and lipoprotein lipase: the loop covering the catalytic site mediates lipase substrate specificity. J Biol Chem 270, 25396-25401.
- van Tilbeurgh et al. 1994a. Lipoprotein lipase. Molecular model based on the pancreatic lipase x-ray structure: consequences for heparin binding and catalysis. J Biol Chem 269, 4626-4633.
- Merkel et al. 1998a. Lipoprotein lipase expression exclusively in liver. A mouse model for metabolism in the neonatal period and during cachexia. J Clin Invest 102, 893–901.
- Masuno et al. 1984a. Lipoprotein lipase-like activity in the liver of mice with Sarcoma 180. J Lipid Res 25, 419–427.
- Berg ed. 2006a (Book). Biochemistry, chapter 16. W.H. Freeman and Company, NY.
- Lindberg & Olivercrona 2002a. Lipoprotein lipase from rainbow trout differs in several respects from the enzyme in mammals. Gene 292, 213-223.
- Eckel & Robbins 1984a. Lipoprotein lipase is produced, regulated, and functional in rat brain. PNAS 81, 7604-7607.
- Bessesen et al. 1993a. Spinal cord of the rat contains more lipoprotein lipase than other brain regions. J Lipid Res 34, 229-238.
- Wong & Schotz 2002a (Review). The lipase gene family. J Lipid Res 43, 993-999.
- Morley et al. 1975a. Hydrolysis of diacylglycerol by lipoprotein lipase. J Biol Chem 250, 3414-3418.
- Augustus et al. 2003a. Routes of FA delivery to cardiac muscle: modulation of lipoprotein lipolysis alters uptake of TG-derived FA. Am J Physiol Endocrinol Metab 284, E331–E339.